En 1999, el oncólogo español Manuel Hidalgo, que ejercía entonces en la Universidad de Tufts (EEUU), recibió a un ejecutivo coreano, directivo de máximo nivel de la petrolera British Petroleum (BP). A su esposa le habían diagnosticado un cáncer de vesícula, un tumor maligno de muy mal pronóstico, y él estaba decidido a hacer todo lo que estuviera en su mano -y en su bolsillo- para salvarla.
Contactó con Hidalgo para ver qué se podía hacer y el español le devolvió la llamada con una insólita propuesta: quería implantar a un ratón de su laboratorio una porción del cáncer de su mujer. En el animal se probarían las distintas opciones terapéuticas y el resultado ayudaría a predecir qué tratamiento de quimioterapia iba a ser más eficaz para ella.
Una fotografía del empresario, su mujer y su padre se puede ver hoy en el despacho de Hidalgo en el Centro Nacional de Investigaciones Oncológicas (CNIO) en Madrid. La coreana -de quien el médico prefiere no dar el nombre- sigue viva 15 años después de que su marido financiara la copia de su cáncer en otro animal con 600.000 dólares (527.000 euros).
Quien subvenciona ahora las investigaciones de Hidalgo y sus ratones avatar no es un particular, sino el principal organismo público del Viejo Continente en estas lides, el Consejo Europeo de Investigación (ERC, de sus siglas en inglés). A finales de junio, decidió conceder a los investigadores españoles una de sus ayudas más prestigiosas, las ERC Advanced Grants, dotadas con 2,5 millones de euros para los próximos cinco años.
En estos tres lustros, el injerto de tumores personalizados en animales de laboratorio ha pasado de ser una técnica prometedora a una realidad en muchísimos centros de todo el mundo, aunque aún sigue sin poderse afirmar lo que todos los médicos desean: que llevar a cabo esta técnica alarga la vida del paciente. A esta pregunta es a la que tienen ahora que dar respuesta Hidalgo y sus colaboradores, lo que harán con un ensayo clínico en el que se evaluará a 150 pacientes y que está a punto de comenzar.
Por la misma época en que la coreana lograba vencer al cáncer, otro paciente no tuvo la misma suerte. "Era un empresario que se hizo rico vendiendo paracetamol en Polonia. Tenía un condrosarcoma, un tumor rarísimo y de muy mal pronóstico, y David Sidransky [director de investigación de cáncer de cabeza y cuello de la Facultad de Medicina de la Universidad Johns Hopkins] me llamó para que le hiciéramos un avatar; al final murió, pero publicamos un artículo científico con su caso y fue el germen de lo que es ahora Champions", recuerda Hidalgo.
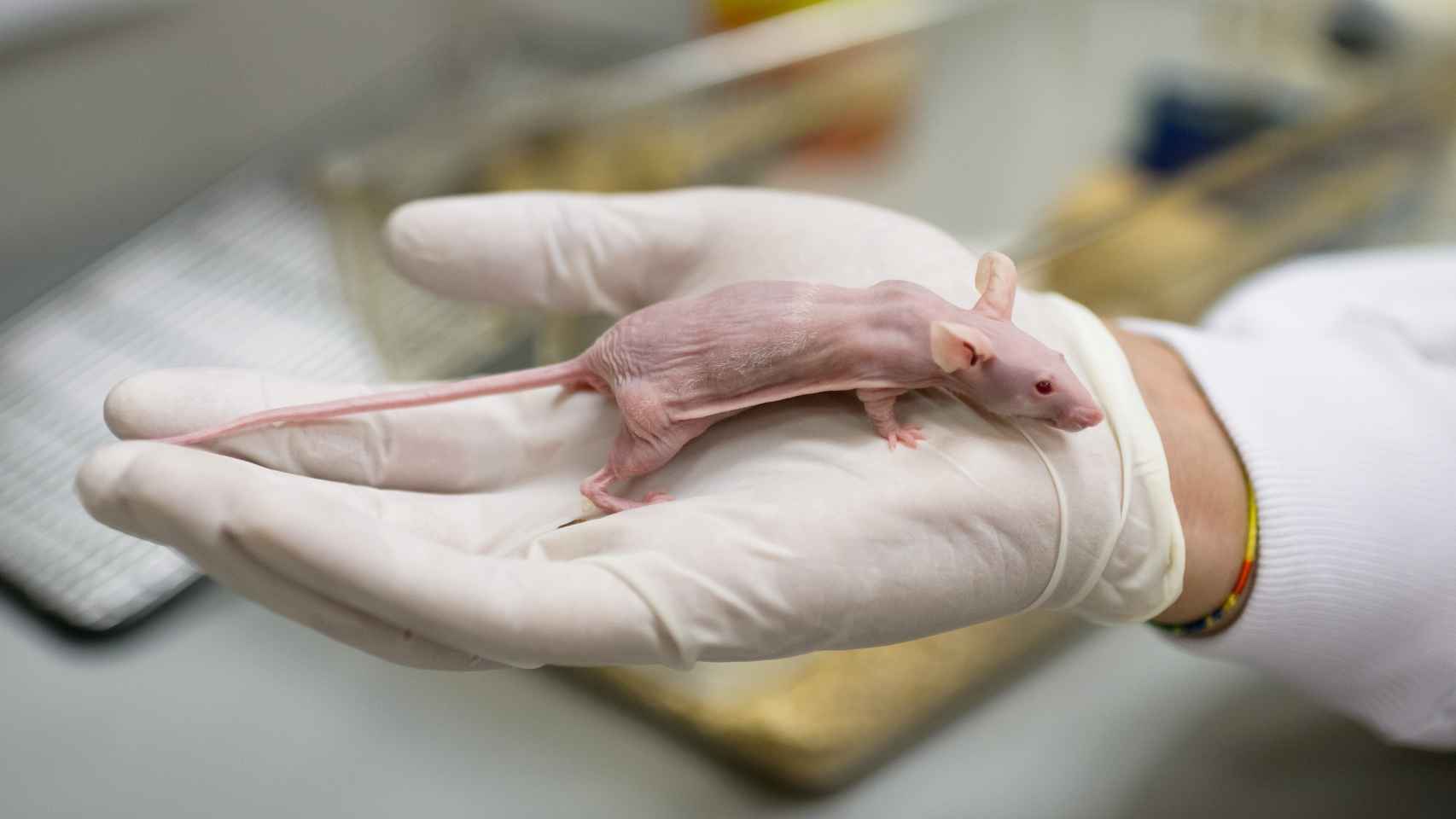
Hidalgo trabaja con ratones avatar en su laboratorio en Madrid
Champions Oncology es una empresa que se autodefine en su página web como "comprometida con el desarrollo de soluciones tecnológicas avanzadas para personalizar el uso de fármacos oncológicos". Ahora mismo, cuenta con cerca de 1.000 ratones injertados con tumores humanos, según confirma Sidransky en conversación telefónica con EL ESPAÑOL.
El sueño de dos oncólogos idealistas es ahora una compañía que cotiza en el Nasdaq, de la que Hidalgo posee un 8%. Sindransky reconoce que los principales clientes de su empresa no son pacientes, sino laboratorios farmacéuticos. "Prácticamente todas las grandes farmacéuticas usan nuestra base de datos; compran el uso de los modelos y de la información que ofrecen y deciden según estos datos probar o no fármacos en investigación", comenta el médico estadounidense.
En España existe una compañía con un perfil similar aunque obviamente más pequeña. Xenopat es una empresa público-privada, una spin-off del Instituto Catalán de Oncología (ICO), el Instituto de Investigación Biomédica de Bellvitge (IDIBELL) y el Hospital Universitario de Bellvitge (HUB).
Pero la generación de modelos de ratón con cáncer está lejos de estar tan extendida como en Estados Unidos, donde cualquier paciente que pueda permitírselo puede encargar uno de estos avatares con "su" cáncer. Lo comenta Héctor Palmer, responsable del Laboratorio de Células Madre y Cáncer del Vall d'Hebron Institute of Oncology (VHIO, en Barcelona), otro de los centros donde se investiga con estos animales. "En EEUU sí es un negocio; hay pacientes que se niegan a entrar en un ensayo clínico hasta saber si su ratón responde o no al fármaco que se está probando", comenta.
En España, denuncia este oncólogo, "la financiación pública es minúscula, pero sí hay interés por parte de las compañías farmacéuticas, que dan bastante libertad, porque lo que les interesa es que haya modelos".
Los pasos del experimento
1.- Elegibilidad. En el ensayo clínico que financia el ERC, los participantes están muy acotados. Son enfermos de cáncer de páncreas avanzado, inoperable, a los que se les ha podido extraer parte del tumor mediante una biopsia.
Otros laboratorios, como el de Palmer, trabajan con más tipos de pacientes: afectados por cáncer colorrectal a los que se ha efectuado cirugía con intención curativa, enfermos de este mismo tipo de tumor pero metastásico y personas que participan en ensayos clínicos para distintos medicamentos.
En EEUU la variabilidad es mucho mayor. "Hay incluso oncólogos que lo ofrecen a pacientes de buen pronóstico, sólo por si acaso", comenta Sidransky.
2.- El proceso. Una vez diagnosticado, el enfermo comienza a recibir el tratamiento convencional. Al mismo tiempo, sus médicos le someten a una biopsia, aunque ya se haya hecho una para el diagnóstico. "El tejido tiene que estar fresco", recuerda Hidalgo.
De parte del fragmento se extrae el ADN para la secuenciación del tumor. El resto se inyecta bajo la piel de "cinco o diez ratones" y, en más del 80% de los casos, crece. "Esto no es suficiente para hacer un experimento, hacen falta más animales, a los que implantas el cáncer de los primeros según se va desarrollando".
Al final, se llegan a tener 80 ó 90 ratones con el tumor original del paciente.
3.- La búsqueda de los fármacos. Una vez secuenciado el genoma, se buscan los fármacos que más se puedan ajustar al tumor. Fátima Al-Shahrour, bioinformática del CNIO, lo explica: "Se secuencia el tumor y la sangre del paciente y se ve qué es lo que tiene el cáncer que no tiene la secuencia normal".
"A continuación, se incluyen los resultados en una base de datos, en nuestro caso una desarrollada por nosotros mismos, PanDrugs; la herramienta ofrece ciertos fármacos candidatos y nosotros los priorizamos. En primer lugar, los que están aprobados por las autoridades sanitarias; en segundo, los que se están probando en ensayos clínicos y, por último, los que están en fase experimental", comenta Al-Shahrour, que incide en que el secreto está en "hacer metodologías de predicción". Es decir: averiguar en el ordenador qué fármaco funcionará en el ratón y tendrá, por tanto, más posibilidades de ser eficaz en el paciente.
"Normalmente, se proponen de dos a cinco medicinas; el avatar es costoso técnica y económicamente, y no se pueden ofrecer demasiadas propuestas", resalta la experta del CNIO.
Tras todo este procedimiento, el oncólogo responsable del experimento recibe los resultados y decide aplicarlos o no a los ratones. "Los bioinformáticos te hacen la propuesta, algunas son muy obvias, otras claramente erróneas. No es un procedimiento automático", comenta Hidalgo.
Los usos de la información
Los "ratones avatar" tienen varias utilidades. La primera es obvia y es mejorar la supervivencia de pacientes con muy mal pronóstico. Palmer es algo pesimista sobre lo que se ha logrado en la actualidad. "Hemos conseguido predecir la respuesta, pero es una carrera contrarreloj y todavía no hemos llegado a tiempo", resume el oncólogo del centro catalán.
Su colega Hidalgo es más optimista. En su haber, un paciente de cáncer de páncreas -con una tasa de mortalidad altísima- que sobrevivió siete años, seis y medio más de la expectativa con la que llegó a su consulta.
En el otro extremo del optimismo, Sidransky: "Recuerdo otro de los primeros casos, un hombre con cáncer oral al que sus médicos desahuciaron tras la cirugía y decidió irse a morir a una isla. Afortunadamente, nos consultó antes. Tras el análisis genómico, se descubrió que tenía una mutación en el gen EGFR y el ratón confirmó que respondería a un anticuerpo [un tipo de fármaco oncológico] y a radioterapia. Lleva 11 años vivo".
Lo que se pretende conseguir con los xenoinjertos derivados de paciente (los avatares en lenguaje científico) es simple y complicado a la vez. Se trata de ganar tiempo. En situaciones normales, un enfermo de cáncer se somete a un tratamiento. Si el cáncer recurre (algo que ocurrirá en la mayoría de los de mal pronóstico), se le administrará un tratamiento de segunda línea. Cuando éste fracase, se intentará -si lo hay- con un tercer medicamento, y así hasta que no haya más opciones. Es algo que habitualmente se hace a ciegas, basándose en ensayos clínicos generalizados y no en el tumor concreto del paciente.
Los tumores se insertan bajo la piel de los ratones
Pero el cáncer en los ratones avanza mucho más rápido. Hidalgo acota los tiempos: "Se inserta el tumor, que tarda en crecer 10 ó 15 días. Se empieza a tratar con un medicamento y en 28 días, sabemos si éste funciona o no". En el cáncer de páncreas humanos, sin embargo, se tarda seis meses en averiguar lo mismo.
Más allá de alargar la supervivencia del enfermo, el uso de este tipo de modelos tiene otras muchas aplicaciones. "No sólo reproducimos la respuesta terapéutica, sino que sabemos por qué. El ratón no sólo ofrece información para elegir tratamiento, sino para evaluar la progresión", comenta Palmer.
Las compañías farmacéuticas y biotecnológicas también se benefician de las bases de datos que genera el conocimiento aportado por los animales.
El futuro
Todos los expertos consultados para este reportaje tienen claro que el uso de xenoinjertos en ratones es una técnica con futuro y también que hay flecos que solucionar. El primero está en los propios ratones.
Hasta ahora, lo habitual es utilizar ratones inmunodeprimidos, a los que se ha modificado en el laboratorio para que no tengan defensas. De esta forma, su organismo no reacciona contra el cáncer ajeno. De hecho, se empezó usando para estos experimentos a ratones nude, que aún mantenían algo de inmunidad, pero pronto se pasó a los más inmunodeficientes hasta la fecha, conocidos como NSG. Así se ha conseguido un gran éxito a la hora de que los tumores se repliquen en el organismo del ratón.
Sin embargo, esta gran ventaja se vuelve desventaja para probar una de las terapias más prometedoras en la lucha contra el cáncer, la inmunoterapia. Estos tratamientos funcionan modificando las defensas del organismo para enseñarle a luchar contra su propio cáncer. Lógicamente, los ratones avatar no sirven para probarlas, porque no cuentan con dicho sistema inmune. "Acabo de desarrollar con Ignacio Melero, de la Clínica Universidad de Navarra, un ratón inmunocompetente, al que pusimos sangre del paciente; los linfocitos crecieron dentro del ratón y logramos un animal con el sistema inmune del enfermo; pero se trata de una técnica que todavía tiene poco éxito", comenta Hidalgo.
El segundo fleco está en cómo se reproducen los tumores. Precisamente para poder observar cómo se comportan y cómo responden a los tratamientos, lo habitual es injertar el cáncer bajo la piel del ratón. Así, la réplica no es exacta, porque el tumor no está anatómicamente en el mismo lugar que en el enfermo. Eso impide, por ejemplo, analizar el comportamiento de las metástasis.
Como explica Palmer, ya se ha desarrollado una solución para este problema y son los llamados ortoxenoinjertos. El fragmento del tumor humano se inserta en el mismo órganos de origen en el ratón. Es lo que llevan a cabo en la empresa Xenopat, aunque el propio Palmer reconoce que dichos experimentos "son más difíciles según la progresión del tumor".
A pesar del papel destacado de los ratones en este área de investigación, existe la posibilidad de que en un futuro el procedimiento pueda llevarse a cabo sin animales, lo que sin duda abarataría el coste. "Puede que sea posible llevarlo a cabo en un derivado de células del paciente que se conviertan en organoides [órganos artificiales creados a partir de células madre reprogramadas, aún en fase de investigación] que crezcan en una placa de Petri, es algo que se está empezando a estudiar", señala Palmer.
Hidalgo está de acuerdo. "Estamos en la versión 1.0; hay mucho que mejorar en cuanto a rapidez y a modelos donde probar los fármacos".
El coste
Pero si hay un obstáculo que dificulta la investigación con este sistema es el económico. Hasta recibir la ayuda europea, Hidalgo se financió gracias a donaciones particulares (sobre todo en Estados Unidos) y al apoyo de dinero filantrópico. "La Fundación Cris contra el Cáncer nos dio más de 100.000 euros para empezar y con ello financiamos el primer estudio, en el que tratamos a 20 pacientes", recuerda Hidalgo.
El coste de los experimentos se ha reducido considerablemente desde los inicios de la técnica. Sidransky comenta que actualmente cuesta alrededor de 1.500 dólares (1.300 euros), pero con el estudio asciende a 10.000, en EEUU.
En España aún no es una práctica habitual para los pacientes, por lo que es difícil cuantificarlo. La tecnología es la gran responsable del coste, pero los animales son una parte importante del mismo. Según explican en el CNIO, cada ratón NSG cuesta 145 euros, a lo que hay que sumar el transporte, ya que los traen de empresas situadas fuera de España.
Los ratones tardan menos en responder a la terapia.
Por último, hay que tener en cuenta los fármacos. Los medicamentos oncológicos son muy costosos. Aunque Hidalgo reconoce que en la mayoría de los casos son cedidos por los laboratorios, comenta que usan ciertas estrategias para abaratar costes: "A veces busco pastillas que le sobren a pacientes. La familia de una afectada que desgraciadamente acaba de fallecer me ha mandado 20 cápsulas de crizotinib [un fármaco para el cáncer]; con eso tengo para todos los estudios. Para los inyectables, busco lo que sobra en las farmacias hospitalarias. Si un paciente necesita por ejemplo 450 mililitros de un fármaco, se abren dos viales de 250 y sobran 50, que normalmente se tiran".
El problema de la financiación se solventará si el proyecto que dirige Hidalgo da resultados positivos y se demuestra de forma fehaciente que la utilización de ratones avatar aumenta la supervivencia. También lo podrán hacer otros ensayos clínicos en marcha en todo el mundo.
Al-Shahrour tiene claro que ella se haría un ratón avatar si llegara el caso y se lo pudiera permitir. "Está claro que es un tema económico, pero creo que te abre unas posibilidades, que aumenta opciones. Hasta que no se haga el estudio extensivo no vamos a saber si es una gran ventaja. Yo no creo que usar un ratón avatar vaya a suponer un aumento del 80% de posibilidades de supervivencia en general, sino que lo hará en casos muy personales y específicos", resume.
Sidranksy concluye en su línea optimista habitual. "Por supuesto que sí me haría uno. De hecho, muchos de nuestros clientes son derivados de oncólogos que creen en este proyecto y lo recomiendan casi de forma personal".
La voz del paciente
La mujer de un empresario y expolítico ibicenco (que prefiere no dar su nombre) es una de las pocas personas que ha participado en un experimento con ratones avatar. Ella no ha querido hablar para este reportaje: su estado de salud es delicado y el xenoinjerto no ha sido en ella todo lo beneficioso que su marido y su médico querían.
Pero este último ha optado por relatar su experiencia a este diario. Lejos de estar resentido, subraya que su oncólogo, Manuel Hidalgo, les advirtió desde el principio que los resultados "serían a largo plazo" y que "no estaban garantizados". "También nos dijo que podría beneficiarse otra gente distinta a mi esposa".
La odisea de esta mujer comenzó en una consulta de atención primaria, donde un médico de familia advirtió unos nódulos en el páncreas que "valdría la pena analizar". El matrimonio decidió tratarse en el Hospital Madrid Sanchinarro, donde le realizaron un PET-TAC que desveló un cáncer detectado, en teoría, a tiempo.
"El tumor se operó; se quitó la parte afectada y un margen de seguridad y se le dieron sesiones de quimioterapia por si habían quedado microcélulas", comenta su marido. Al cabo de un año, se vio que la estrategia no había funcionado y las células tumorales habían proliferado a la glándula suprarrenal, donde formó tumores pequeños y de poca actividad. Cuando la radioterapia tampoco funcionó, Hidalgo les propuso financiar la creación de ratones avatar. "Donamos alrededor de 40.000 euros y sabíamos que podía no funcionar".
El análisis de los datos arrojó varios fármacos idóneos. "La mayoría ralentizaba el crecimiento pero no reducía el tumor; sólo dos lo hacían y nos centramos en ello", recuerda el empresario.
Mientras que uno de los dos medicamentos produjo reacciones muy adversas a su mujer, el otro se le pudo administrar con normalidad. Ahora están a la espera, aunque las expectativas no son muy halagüeñas. "Uno de los argumentos que nos dio el Dr. Hidalgo es que suponía un avance científico", dice.
Sólo a base de éxitos y fracasos se podrá responder a la pregunta de si los avatares son realmente un arma eficaz contra el cáncer. Pero el trabajo no es en vano. Todos los investigadores coinciden en que la información que aportan es y será de suma utilidad. Un fracaso en este campo es a la vez un éxito.