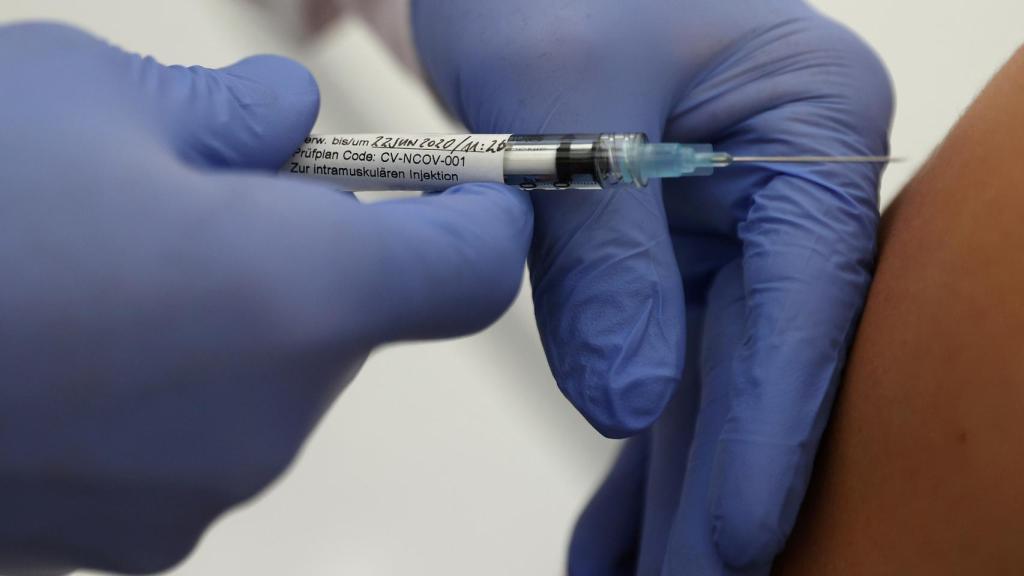
Ensayo clínico de la vacuna de CureVac en la clínica universitaria de Tuebingen (Alemania)
La EMA inicia la revisión de la vacuna de CureVac, primer paso para su aprobación
Bruselas ha firmado un contrato para el suministro de hasta 400 millones de dosis.
12 febrero, 2021 11:46Noticias relacionadas
Una nueva vacuna contra la Covid-19 podría entrar pronto en la cartera de la Unión Europea y contribuir a paliar la actual situación de escasez de dosis. La Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha iniciado este viernes la revisión continua de CVnCoV, el antígeno que está desarrollando la empresa de biotecnología alemana CureVac. Este procedimiento es la antesala para la rápida aprobación de la vacuna, una vez que estén disponibles todos los datos de los ensayos clínicos.
Bruselas ha firmado ya un contrato con CureVac en el que se prevé la compra inicial de 225 millones de dosis, además de la opción de solicitar hasta 180 millones de dosis adicionales, que se suministrarán una vez que la vacuna haya demostrado ser segura y eficaz contra el coronavirus. A España le corresponderían alrededor del 10% del total, es decir, hasta 40 millones de dosis.
La EMA ha decidido iniciar la revisión continua de la vacuna de CureVac basándose en los resultados preliminares de los estudios de laboratorio y de los primeros estudios clínicos en adultos. Estos ensayos sugieren que la vacuna desencadena la producción de anticuerpos y células inmunes que atacan al SARS-CoV-2, el virus que causa COVID-19. El antígeno de CureVac se basa en la misma tecnología de ARN mensajero que las de Pfizer-BioNTech y Moderna, que ya han sido autorizadas por la UE.
Actualmente, la compañía está realizando ensayos de fase 3 en personas para evaluar la seguridad, inmunogenicidad (qué tan bien desencadena una respuesta contra el virus) y efectividad de la vacuna contra COVID-19. La EMA evaluará los datos de estos y otros ensayos clínicos a medida que estén disponibles. La revisión continua continuará hasta que haya suficiente evidencia disponible para una solicitud formal de autorización de comercialización.
Además del anticipo pagado por Bruselas tras las firma del contrato (cuyo importe no es público), el Banco Europeo de Inversiones concedió el pasado 6 de julio un préstamo de 75 millones para el desarrollo y producción a gran escala de vacunas. Un movimiento que se produjo tras el intento del ex presidente de Estados Unidos, Donald Trump, de hacerse con la exclusividad de la vacuna de CureVac contra el coronavirus.
CureVac ha alcanzado un acuerdo con el gigante farmacéutico Bayer, que no ha desarrollado ningún antídoto propio, para fabricar su vacuna contra la Covid en Alemania. En total, Bayer tiene previsto entregar 160 millones de pinchazos extra de CureVac a lo largo de 2022.
De momento, la EMA ha dado luz verde a tres vacunas: la de Pfizer, la de Moderna y la de AstraZeneca. La siguiente en aprobarse será probablemente la de Janssen en las próximas semanas. Además, la Agencia tiene en revisión continua el antígeno de Novavax (compañía con la que Bruselas negocia un contrato por 200 millones de dosis) y desde este viernes el de CureVac.
En contraste, la EMA ha insistido esta semana en que no ha recibido ninguna solicitud para autorizar la vacuna rusa Sputnik V, ni siquiera para someterla a revisión continua. Además, la Comisión Europea ha reiterado que no tiene ninguna intención de incorporarla a su cartera de antígenos, pese a que Hungría ha empezado a utilizarla por su cuenta.
La presidenta de la Comisión, Ursula von der Leyen, ha repetido este viernes que mantiene su objetivo de que el 70% de la población adulta de la UE esté vacunada para el final del verano, lo que permitiría alcanzar la inmunidad de grupo y acabar con la pandemia. El final del verano es el 21 de septiembre, ha precisado la presidenta.





