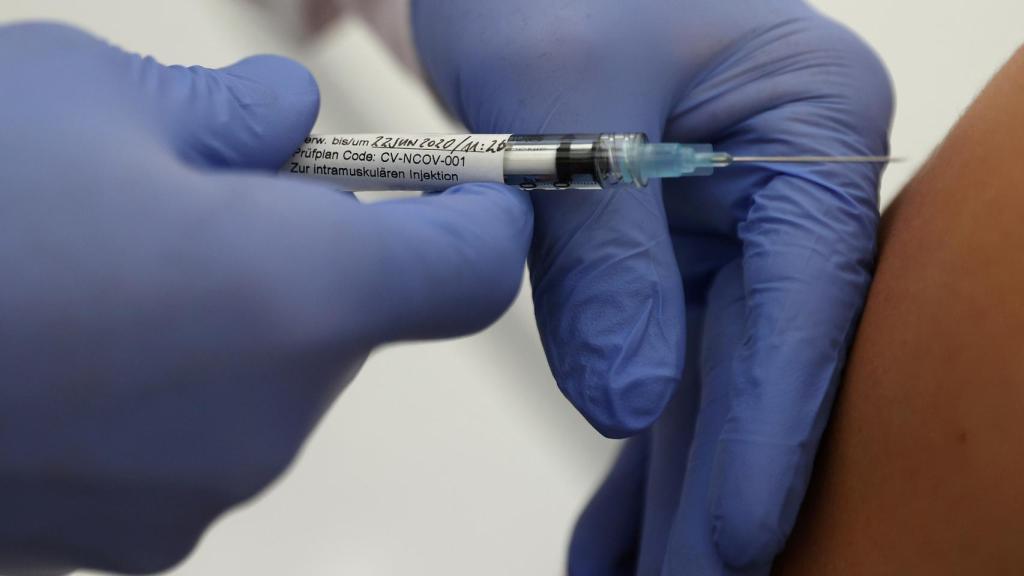
Ensayo clínico de la vacuna de CureVac en la clínica universitaria de Tuebingen (Alemania)
CureVac renuncia a su vacuna contra la Covid-19 tras sus malos datos de eficacia
La farmacéutica alemana se centrará en el desarrollo de un candidato de segunda generación junto a GSK.
12 octubre, 2021 15:56Noticias relacionadas
- El Gobierno aprueba la compra de dos millones de dosis de la vacuna contra la Covid de Novavax
- De CureVac a Hipra: estas son las vacunas de segunda generación que están por llegar
- CureVac confía en que su vacuna de segunda generación pueda reducir la transmisión del virus
- A la Unión Europea le sobran vacunas: ha comprado dosis para inmunizar cinco veces a su población
La farmacéutica alemana CureVac ha anunciado este martes que renuncia a seguir adelante con su vacuna contra la Covid-19 después de que los ensayos clínicos desvelaran una baja tasa de eficacia del 48%. El laboratorio se ha retirado del proceso de autorización iniciado por la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) y ha cancelado el contrato de compra anticipada que había firmado con la Comisión Europea por hasta 400 millones de dosis.
CureVac justifica esta maniobra por la necesidad de centrar todos sus esfuerzos en la vacuna de segunda generación, basada en la tecnología del ARN mensajero, que ya está desarrollando junto con la farmacéutica GSK. Una inyección que espera tener lista para el año 2022.
Basándose en su comunicación más reciente con la EMA, el laboratorio argumenta que la aprobación de su vacuna de primera generación contra la Covid-19 no se produciría, como muy pronto, hasta el segundo trimestre de 2022. Es decir, llegaría tarde para hacer frente a la etapa más urgente de la pandemia.
Además, para ese momento, CureVac y GSK esperan estar ya en una fase avanzada del desarrollo de la vacuna de segunda generación, cuyo objetivo es adaptarse a las nuevas variantes y a la nueva normalidad endémica del virus.
Calidad y eficacia
Por su parte, la EMA ha confirmado que pone fin a la evaluación continua de la vacuna de CureVac, que había iniciado en febrero de 2021. En el momento de la retirada del laboratorio, el regulador europeo había recibido datos no clínicos (de laboratorio), datos de estudios clínicos en curso, datos sobre la calidad y el proceso de fabricación de la vacuna y el plan de gestión de riesgos (RMP).
"Aunque la EMA estaba acelerando la revisión de los datos, algunos interrogantes sobre la calidad de la vacuna, que impactaban en el balance beneficio-riesgo, y el hecho de que los resultados del estudio principal mostraban solo una modesta eficacia de la vacuna en adultos, todavía tenían que afrontarse de forma satisfactoria", ha dicho el regulador europeo en un comunicado.
Las personas que hayan participado en ensayos clínicos con la vacuna de CureVac y tengan preguntas sobre su estado de vacunación, el certificado COVID digital de la UE o las restricciones de viaje asociadas con la vacunación deben ponerse en contacto con las autoridades pertinentes de su país de residencia, aconseja la EMA.
La vacuna original de CureVac se basaba también en la tecnología del ARN mensajero. Pero a diferencia de las inyecciones de Pfizer-BioNTech y Moderna, cuya tasa de eficacia supera el 90%, el ARNm se utilizaba sin modificar.
La "consecuencia directa" del abandono de esta vacuna es que el acuerdo firmado con Bruselas para suministrar hasta 400 millones de dosis queda sin efecto. El laboratorio asegura que se mantiene en contacto con la Comisión Europea para evaluar la posibilidad de aprovechar los compromisos adquiridos para su vacuna de segunda generación. Curevac firmó en julio del año pasado un contrato de préstamo de 75 millones de euros con el Banco Europeo de Inversiones para el desarrollo y la producción a gran escala de vacunas.
La Comisión Europea no ha querido desvelar cuánto dinero adicional pagó a la farmacéutica como adelanto, una cantidad que se perderá ahora definitivamente. "Desde el lanzamiento de nuestra estrategia de vacunas y la conclusión de los acuerdos con los laboratorios, siempre estuvo claro que existía un grave riesgo de que no todos los candidatos a vacunas recibieran la luz verde de la EMA", ha explicado un portavoz a EL ESPAÑOL.
"Por lo tanto, cuando un candidato no pasa la prueba, eso demuestra exactamente que nuestro enfoque cuidadoso funciona y que la evaluación exhaustiva por parte de la EMA es una piedra angular de nuestra estrategia", ha zanjado el portavoz.
Bruselas sostiene que su estrategia de construir una cartera de vacunas diversificada ha dado frutos. Un total de cuatro vacunas han sido autorizadas en la UE: Pfizer, Moderna, AstraZeneca y Janssen. Y hasta ahora 800 millones de dosis han sido entregadas a los Estados miembros y otros 900 millones de dosis se han exportado a países fuera de la Unión.





