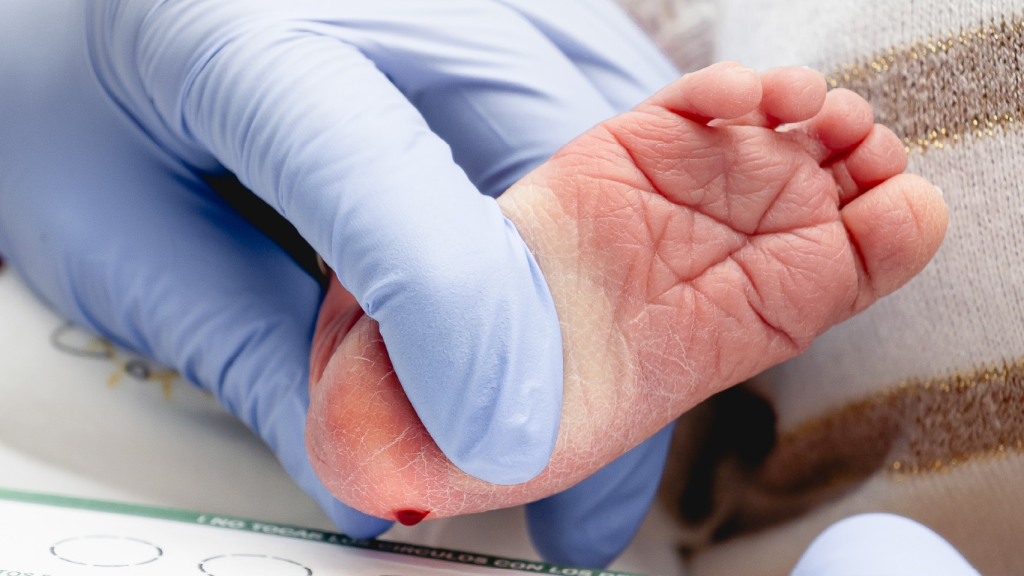
Cribado neonatal.
La victoria contra la atrofia espinal en España: del tratamiento pionero con polémica a salvar vidas de niños
La terapia de vanguardia inspiró la inclusión de la patología en el cribado neonatal tras aplicar una terapia de vanguardia. Pese al éxito, fue denunciada.
Más información: La Generalitat pide a una madre que devuelva 362,63 euros de ayuda a la dependencia tras la muerte de su hijo de 12 años
España ha dado un paso de gigante para equipararse con otros países de Europa en materia de cribado neonatal, la famosa 'prueba del talón' que se realiza a los recién nacidos para detectar enfermedades congénitas. La Comisión de Salud Pública del Consejo Interterritorial del Sistema Nacional de Salud (CISNS) aprobaba el pasado 23 de enero incluir cuatro nuevas patologías en el cribado, entre ellos una antigua reivindicación: el de la atrofia muscular espinal (AME).
"La cartera común pasa de incluir 7 a 23 enfermedades en un año. Y seguiremos ampliando", celebraba la ministra de Sanidad, Mónica García. Las otras tres enfermedades recién incluidas, que se examinarán buscando marcadores en una muestra de sangre obtenida del talón en las primeras 24-72 horas de vida, serán la acidemia isovalérica, inmunodeficiencia combinada grave y la aciduria 3-hidroxi-3-metilglutárica.
Sin embargo, la atrofia muscular espinal ha sido un caballo de batalla para la ampliación del cribado. Se trata de una enfermedad rara que afecta a 4 de cada 100.000 españoles y condena a un rápido deterioro: en el caso de la atrofia de tipo uno, la más grave, el 80% de los niños no sobreviven al primer año. La esperanza llegó en 2021 con la aprobación en España de Zolgensma (Onasemnogén Abeparvovec). Pero su coste por paciente es de más de dos millones de euros.
Hay otros dos tratamientos aprobados en nuestro país: Nusinersen (Spinraza) y Risdiplam (Evrysdi). Sin llegar a las cifras exorbitantes del Zolgensma, tienen un coste que supera los 200.000 euros anuales. Pacientes que lo han estado recibiendo periódicamente -con mejoras tan cruciales como recuperar la capacidad de andar- han visto cómo se les retiraba, ya que no todas las CC.AA. cubren el coste en España.
Pero Zolgensma está diseñado para usarse una única vez, antes de que se manifiesten los síntomas. Y ahí entra el cribado neonatal, explica a EL ESPAÑOL Rocío Calvo, Neuropediatra del Hospital Universitario de Málaga. Junto a Raquel Yahyaoui, hoy jefa del servicio de Análisis Clínicos del Hospital Regional Universitario de Málaga, detectaron la atrofia de tipo 1 en un recién nacido en 2022 dentro de un programa experimental que evaluaba precisamente la ampliación del cribado
Fue la terapia más cara jamás cubierta por el SAS, y también un éxito mayúsculo. "El niño ha cumplido dos años y medio, y camina", celebra Calvo. Pero poco después, eran denunciadas por la gerente del hospital por presuntas "irregularidades" en su desempeño que habrían retrasado la administración del fármaco. "Fue duro", admite la neuropediatra, que todavía no se explica lo ocurrido. "Quizás buscaban cabezas de turco en caso de que no saliera bien".
Niños que recuperan su futuro
La inclusión de la AME en el cribado neonatal era una exigencia "absolutamente obvia" desde el momento en el que se tienen los recursos para detectarla y los fármacos para tratarla, expone Calvo. "Quién nace con ella la desarrollará seguro. Y hay que dar el Zolgensma en el momento perfecto, antes de que inicien síntomas. Actualmente se diagnostica cuando el niño llega a urgencias con un cuadro respiratorio. Y en ese momento, la pérdida de motoneuronas efectivas ya es irreversible".
Los tres fármacos aprobados contra la enfermedad son terapias de vanguardia, explica, de ahí su precio. Pero no funcionan igual. Nusinersen se aplica de forma intratecal (inyectado en el líquido cefalorraquídeo) cada cuatro meses, y para pacientes que no lo toleran bien, Risdiplam se toma por vía oral a diario. Estos fármacos modifican la expresión de los genes implicados en la AME (SMN1 y SMN2) para que sigan produciendo una proteína indispensable para la supervivencia de las neuronas motoras, y alivian de este modo la sintomatología.
Zolgensma, por el contrario, introduce copias correctas de ambos SMN. "Te mete el gen bueno", resume la neuropediatra. Lo hace mediante un vector viral, lo que implica que el paciente no debe tener defensas desarrolladas, o lo rechazará. "Sólo se puede poner en menores de 9 meses y con menos de 12 kilos". Nada de esto era posible antes del cribado. "Antes solo obteníamos éxitos parciales. Sabíamos que quedarían secuelas". Ahora, estamos ante un verdadero "cambio de paradigma", celebra Calvo.
En medio de esta historia de éxito, el paréntesis de la denuncia interpuesta por la denuncia fue "una cosa absurda", lamenta. La gerencia las reponsabilizaba de que el tratamiento se hubiera alargado dos semanas sobre el plazo inicial de un mes, "precisamente a quienes habíamos luchado para que el paciente se tratara lo más pronto posible". La demanda fue desestimada finalmente por la Fiscalía, que apreció si acaso "exceso de celo en beneficio del paciente".
Desde entonces, una veintena de niños han sido tratados con Zolgensma en España, y otras CC.AA. como Galicia o Madrid han ido añadiendo la atrofia muscular espinal al cribado neonatal antes incluso de la aprobación a nivel interterritorial. Y el debate del coste se zanja desde el momento en el que una única administración evita toda una vida de discapacidad y necesidades hospitalarias intensivas, con el gasto sanitario, social y humano que conlleva. "En España no hemos visto una idiocía debida a la fenilcetonuria en 50 años. Y ha sido gracias al cribado neonatal".